- Eine Immuntherapie soll bewirken, dass das körpereigene Immunsystem die Krebszellen bekämpft. Dabei gibt es unterschiedliche Ansätze und Wirkmechanismen.
- Es gibt bereits verschiedene zugelassene Medikamente und Methoden im Bereich Immuntherapie. Sie kommen vor allem für Krebspatientinnen und -patienten mit fortgeschrittener Erkrankung infrage.
- Dieser Text erläutert, wem eine Immuntherapie helfen kann, wie sie abläuft und welche Nebenwirkungen auftreten können.
Immuntherapie bei Krebs: Wichtiges in Kürze
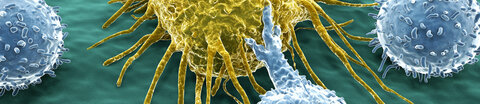
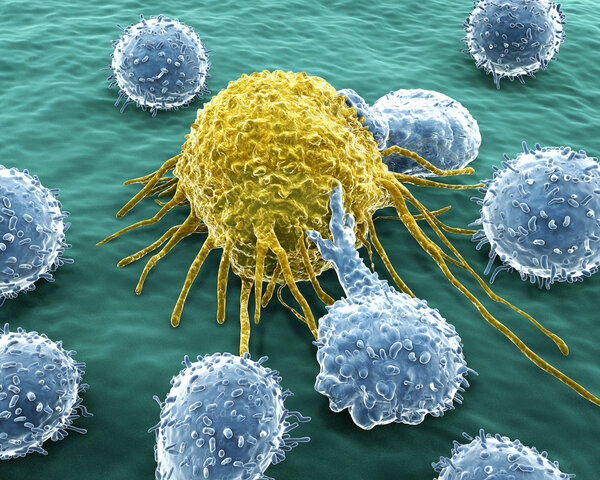
Immuntherapien nutzen das körpereigene Immunsystem, um Krebs zu bekämpfen. Prinzipiell kann das Immunsystem Tumorzellen abtöten. Dafür muss es sie aber erstmal als "fremd" oder "krank" erkennen. Nicht alle Krebszellen sind für das Immunsystem gut erkennbar.
Außerdem verändern sich Krebszellen ständig. Sie können Ausweichstrategien gegen eine Immunantwort entwickeln: zum Beispiel, indem sie sich "unsichtbar" für das Immunsystem machen. Oder indem sie die Immunreaktion hemmen. So können sie dem Abwehrsystem entkommen.
Bei der Immuntherapie werden solche Ausweichmechanismen ausgehebelt. Natürliche Abwehrmechanismen des Körpers werden verstärkt und gezielt auf die Krebszellen gerichtet.
Wer kann eine Immuntherapie bekommen?
Klären Sie Ihre individuelle Situation
Ob bei Ihnen eine Immuntherapie möglich und sinnvoll ist, sollten Sie mit Ihrem behandelnden Ärzteteam besprechen.
Ob eine Immuntherapie infrage kommt, hängt von verschiedenen Faktoren ab, zum Beispiel davon,
- welche Tumorart Betroffene haben,
- wie weit die Erkrankung fortgeschritten ist,
- ob die Krebszellen bestimmte Merkmale tragen – das gilt jedoch nur für manche Tumorarten und Medikamente.
Die meisten Betroffene, die eine Immuntherapie erhalten, haben eine fortgeschrittene Krebserkrankung. Das bedeutet: Ihre Erkrankung ist in der Regel nicht heilbar. Inzwischen erhalten auch manche Patientinnen und Patienten mit Krebs in früheren Stadien eine Immuntherapie.
Was kann man sich von der Immuntherapie erwarten?
Bei einer fortgeschrittenen Krebserkrankung zielt die Immuntherapie darauf ab, die Lebenszeit möglichst zu verlängern und die Lebensqualität zu verbessern.
Es gibt Tumorarten, die häufig gut auf eine Immuntherapie ansprechen und solche, bei denen diese Behandlung bisher seltener oder sogar so gut wie nie funktioniert. Das hängt zum Beispiel davon ab, wie gut das Immunsystem die Krebszellen erkennen kann.
Abhängig von der Krebserkrankung und den individuellen Voraussetzungen gibt es Immuntherapien, die manchen Betroffenen mit fortgeschrittener Erkrankung inzwischen ein Langzeitüberleben ermöglichen.
Wirkmechanismen und Forschung
Klären Sie die Möglichkeit einer Studie
Fragen Sie Ihre Ärztinnen und Ärzte, ob in Ihrer Situation eine klinische Studie infrage kommt.
Es gibt unterschiedliche Methoden, um das Immunsystem dazu zu bringen, den Krebs zu bekämpfen. Die derzeit verfügbaren Therapien setzen an verschiedenen Stellen des Immunsystems an. Am häufigsten eingesetzt werden im Moment Checkpoint-Inhibitoren, gefolgt von der CAR-T-Zelltherapie.
Weitere Ansätze kommen nur selten infrage oder befinden sich noch in der Entwicklung, beispielsweise bispezifische Antikörper oder therapeutische Krebsimpfungen.
Das Feld der Immuntherapien entwickelt sich schnell weiter. Deshalb gibt es viele klinische Studien zu neuen Ansätzen. Außerdem prüfen Forschende, ob und wie sich Immuntherapien mit weiteren Krebsbehandlungen wie Chemotherapie, Strahlentherapie oder anderen Immuntherapie-Methoden kombinieren lassen.
Nicht zugelassene Methoden und kommerzielle Angebote
Es gibt Anbieter, die Mittel zur "Immunstärkung" oder nicht zugelassene Immuntherapien außerhalb von klinischen Studien anbieten. Die Angebote reichen von pflanzlichen Mitteln und Vitaminen zur Immunstärkung bis hin zu Krebsimpfung, dendritischen Zellen oder der "aktiv-spezifischen Immuntherapie".
Häufig gibt es allerdings keine wissenschaftlich nachvollziehbaren Daten zu Wirksamkeit und Risiken der Methoden. Die Kosten werden von den Krankenkassen meist nicht übernommen.
- Experten empfehlen, nicht zugelassene Immuntherapeutika nur unter kontrollierten Bedingungen in klinischen Studien einzusetzen.
- Fragen Sie Ihre behandelnden Ärzte, wenn Sie sich für ein solches Angebot interessieren. Diese können Ihnen dabei helfen, Nutzen und Risiken der Methode einzuordnen.
- Auch der Krebsinformationsdienst informiert – telefonisch oder per Mail – über nicht zugelassene Immuntherapien.
Fragen Sie uns!
Gerne stehen unsere Ärztinnen und Ärzte Ihnen kostenfrei mit Hintergrundinformationen für Ihre individuelle Situation zur Verfügung:
- am Telefon täglich von 8 bis 20 Uhr, unter 0800 – 420 30 40
- per E-Mail an krebsinformationsdienst@dkfz.de oder über ein datensicheres Kontaktformular
Checkpoint-Inhibitoren
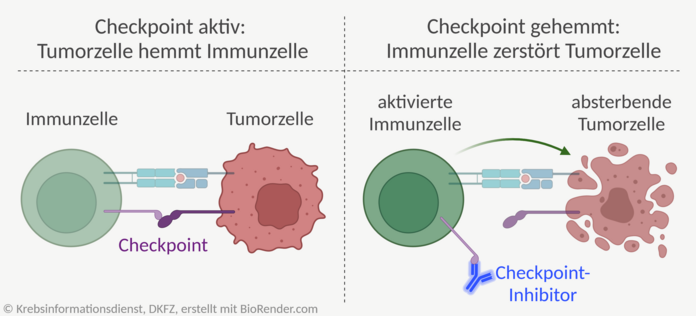
Bild: © Krebsinformationsdienst, DKFZ; angepasst nach "Immune Checkpoint Inhibitor Against Tumor Cell" von BioRender.com (2024), abgerufen von https://app.biorender.com/biorender-templates
Immun-Checkpoint-Inhibitoren sind Medikamente, die sich gezielt gegen "Bremsen" im Immunsystem richten. Diese Kontrollstellen oder englisch "Checkpoints" begrenzen normalerweise die Immunreaktion. Sie sorgen dafür, dass das Immunsystem nicht zu stark reagiert und verhindern, dass gesunde Zellen angegriffen werden.
Ein Ausweichmechanismus von Tumorzellen ist es, solche Checkpoints anzuschalten und damit die Immunantwort zu bremsen. Checkpoint-Inhibitoren, auch Checkpoint-Hemmer genannt, lösen diese "Bremsen" und verstärken damit die Immunantwort gegen Tumorzellen.
Es gibt mehrere unterschiedliche "Checkpoints" im Immunsystem. Sie tragen Namen wie PD-1, CTLA4 oder LAG3. Gegen mehrere dieser Checkpoints gibt es bereits verschiedene Hemmstoffe. Dabei handelt es sich um sogenannte Antikörper, die an den jeweiligen Checkpoint binden und ihn blockieren. Weitere Checkpoint-Inhibitoren werden noch in klinischen Studien untersucht.
Stellenwert: Checkpoint-Inhibitoren werden bereits bei vielen Tumorarten eingesetzt, darunter zum Beispiel schwarzer Hautkrebs, Lungenkrebs oder Kopf-Hals-Tumoren, aber auch bei manchen Betroffenen mit Darmkrebs und Brustkrebs. Ihre Wirkung bei anderen Krebsarten wird in Studien untersucht.
Die meisten Patientinnen und Patienten, die Checkpoint-Hemmer erhalten, haben bereits eine fortgeschrittene Krebserkrankung. Bei manchen Krebsarten kommen sie aber auch bei einem örtlich begrenzten Tumor infrage.
Checkpoint-Hemmer wirken nur bei einem Teil der Betroffenen. Zeigt sich allerdings eine Wirkung, dann kann diese lange anhalten. Es gibt sogar Betroffene, bei denen sich der Tumor ganz zurückgebildet hat. Momentan wird an Biomarkern geforscht, die vorhersagen sollen, wem eine solche Therapie helfen kann und wem nicht. Hierzu ist aber noch weitere Forschung nötig.
Ablauf der Therapie: Die meisten Patientinnen und Patienten erhalten die Medikamente über eine Vene als Infusion. Die Abstände der Infusionen und die Behandlungsdauer unterscheiden sich je nach Medikament und Krebsart. Selten ist es auch möglich, das Medikament als Spritze unter die Haut zu bekommen.
Je nach Situation erhalten Krebserkrankte ein einzelnes Medikament oder eine Kombination von mehreren Checkpoint-Inhibitoren, oder Onkologen kombinieren die Checkpoint-Hemmer mit anderen Therapien. Betroffene sollten mit ihren Ärzten besprechen, wie ihre Behandlung konkret geplant ist.
Nebenwirkungen: Beschwerden beruhen vor allem auf überschießenden Immunreaktionen. Dazu gehören Fieber, Ausschläge und Juckreiz an der Haut, aber auch Entzündungen des Darms, der Leber, der Nieren oder Hormon-produzierender Drüsen wie der Schilddrüse.
Was lässt sich dagegen tun? Ärzte können, wenn nötig, Medikamente gegen die Beschwerden verschreiben. Manche Patientinnen und Patienten müssen die Behandlung mit den Checkpoint-Hemmern vorübergehend unterbrechen. Bei schweren Nebenwirkungen entscheidet das Behandlungsteam manchmal, die Immuntherapie ganz abzubrechen.
CAR-T-Zelltherapie und ähnliche Ansätze
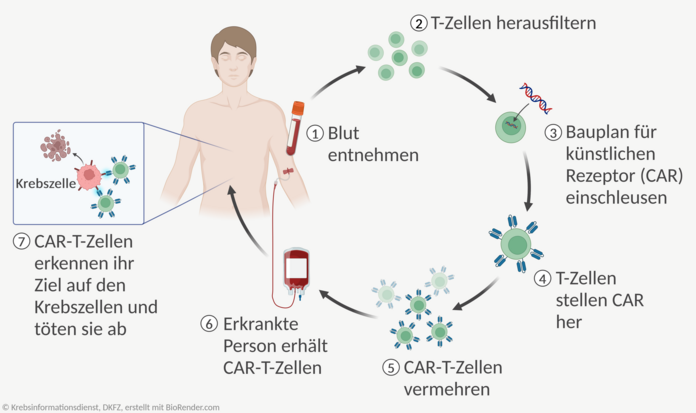
Bild: © Krebsinformationsdienst, DKFZ, angepasst nach "Chimeric Antigen Receptor (CAR) T Cell Therapy: Vein-to-Vein Process" von BioRender.com (2024), abgerufen von https://app.biorender.com/biorender-templates
Bei der CAR-T-Zelltherapie werden körpereigene Immunzellen so umprogrammiert, dass sie Krebszellen erkennen und abtöten können. Die Immunzellen heißen T-Zellen. Sie sind normalerweise im Körper dafür zuständig, erkrankte Zellen zu vernichten.
In die T-Zellen wird der Bauplan für eine künstliche Erkennungsstelle (Rezeptor) eingeschleust, die Merkmale auf den Tumorzellen erkennen kann. Dieser Rezeptor heißt chimärer Antigen-Rezeptor (CAR). T-Zellen, denen der Bauplan eingeschleust wurde, tragen den Rezeptor auf ihrer Oberfläche. Sie werden CAR-T-Zellen genannt. Mithilfe des künstlichen Rezeptors erkennen die CAR-T-Zellen die Tumorzellen und töten diese ab.
Stellenwert: Bisher kommt eine CAR-T-Zell-Therapie vor allem für Patientinnen und Patienten mit Blutkrebserkrankungen (Leukämien und Lymphome) infrage. Allerdings ist die Therapie nicht bei jeder Blutkrebsart und nicht zu jedem Zeitpunkt möglich. Sie ist vor allem für Betroffene nach einem Krankheitsrückfall zugelassen und wenn andere Therapien nicht mehr wirken.
Das Verfahren ist sehr aufwendig, kann aber bei manchen Patientinnen und Patienten die Erkrankung langfristig eindämmen. Mittlerweile liegen die ersten Therapien 10 Jahre zurück. Bei einzelnen der ersten therapierten Lymphomerkrankten trat auch nach dieser Zeit kein Krebs mehr auf. Bei diesen Patientinnen und Patienten sprechen Fachleute sogar von einer möglichen Heilung.
Wissenschaftlerinnen und Wissenschaftler forschen an weiteren Zielstrukturen auf den Tumorzellen, an Möglichkeiten, CAR-T-Zellen auch bei Tumorerkrankungen wie Lungen-, Brust- oder Magenkrebs einzusetzen und an ähnlichen Verfahren mit anderen Immunzellen.
Ablauf der Therapie: Eine CAR-T-Zell-Therapie wird nur in spezialisierten Zentren angeboten. Die Behandlung findet einmalig statt. Als Patientin oder Patient bekommt man dafür zunächst Blut abgenommen, aus dem die Immunzellen herausgefiltert werden. Diese werden an ein spezialisiertes Labor gesendet, dort mit dem Bauplan für den CAR versehen und vermehrt.
In der Regel dauert es mehrere Wochen, bis die fertigen CAR-T-Zellen zur Verfügung stehen. In der Zwischenzeit behandeln die Ärztinnen und Ärzte Krebserkrankte, wenn notwendig, mit einer überbrückenden Therapie.
Bevor Betroffene die CAR-T-Zellen erhalten, bekommen sie eine kurze Chemotherapie. Diese soll das körpereigene Immunsystem zurückdrängen, damit die CAR-T-Zellen sich besser vermehren können.
Da unter Umständen starke Nebenwirkungen auftreten können, muss das Ärzteteam die Patientin oder den Patienten sorgfältig überwachen. Das bedeutet, dass man in der Regel etwa 2 Wochen stationär in der Klinik bleibt.
Nebenwirkungen: Häufig kommt es zu einer überschießenden Immunreaktion mit Fieber, Schüttelfrost und weiteren Symptomen, die bei manchen Betroffenen sehr stark sein können. Werden durch die Behandlung schnell viele Krebszellen zerstört, dann kann das zu verschiedenen Stoffwechsel-Problemen führen.
Auch Nebenwirkungen im Nervensystem wie Kopfschmerzen, Schwindel oder Verwirrtheit können auftreten. Langfristig kann es durch die Therapie zu einer verringerten Menge Immunzellen kommen. Betroffenen neigen dann zu häufigen Infekten.
Was lässt sich dagegen tun? Viele der Nebenwirkungen können Ärztinnen und Ärzte gezielt behandeln oder mit Medikamenten vorbeugen. Bei sehr starken Nebenwirkungen müssen Betroffene manchmal vorübergehend auf der Intensivstation behandelt werden.
Bispezifische Antikörper
Bispezifische Antikörper sind Eiweiße mit 2 verschiedenen Bindungsstellen:
- Die eine bindet meistens ein Merkmal auf einer Tumorzelle,
- die andere bindet und aktiviert abtötende Immunzellen.
Die Immunzellen werden so direkt auf die Tumorzellen gelenkt. Es gibt weitere ähnliche Medikamente mit einem vergleichbaren Wirkmechanismus, zum Beispiel sogenannte BiTe-Antikörper (englisch: Bi-specific T-cell engagers).
Stellenwert: Es gibt bereits mehrere zugelassene Medikamente, zum Beispiel für manche Patientinnen und Patienten mit Leukämie, Lymphom oder Lungenkrebs.
Ablauf der Therapie: Die Antikörper erhalten Patientinnen und Patienten als Infusion in eine Vene oder als Spritze unter die Haut. Die Abstände zwischen den Infusionen/Spritzen und die Behandlungsdauer unterscheiden sich je nach Medikament und Krebsart.
Nebenwirkungen: Die meisten Nebenwirkungen beruhen auf einer zu starken Reaktion des Immunsystems. Dazu gehören beispielsweise Fieber, Übelkeit, Schmerzen, niedriger Blutdruck und Veränderungen im Blutbild.
Antikörper als Medikamente
Antikörper sind Teil des Immunsystems. Sie werden von spezialisierten Blutzellen gebildet. Sie erkennen Fremdstoffe und aktivieren das Immunsystem.
In der Krebsmedizin werden viele verschiedene künstlich hergestellte Antikörper eingesetzt. Dabei nutzt man ihre Eigenschaft, sehr genau ein bestimmtes Merkmal erkennen zu können.
Ein Beispiel sind Checkpoint-Inhibitoren. Auch viele zielgerichtete Medikamente sind Antikörper.
mRNA-Impfung und weitere Krebsimpfungen
Eine therapeutische Impfung soll das Immunsystem gezielt auf die Tumorzellen lenken. Das bedeutet: Dem körpereigenen Immunsystem soll beigebracht werden, die Tumorzellen an bestimmten Merkmalen selbst zu erkennen und sie zu bekämpfen.
Diese Merkmale heißen Tumorantigene. Indem sie dem Immunsystem zusammen mit Wirkverstärkern gezeigt werden, können sie die Immunabwehr aktivieren. Diese soll dann auch Tumorzellen mit dem entsprechenden Merkmal erkennen und abtöten.
Lexikon
Tumorantigen: Krebstypisches Merkmal, das auf gesunden Zellen nicht oder nur in geringen Mengen vorkommt. Normalerweise handelt es sich um Eiweiße, die eine Zelle herstellt, weil sich das zugehörige Erbmaterial verändert hat.
Es gibt verschiedene Möglichkeiten, ein solches Tumorantigen in den Körper zu bringen:
- Proteinbasierte oder Peptid-Impfung: Der Impfstoff beinhaltet das Eiweiß des Tumorantigens selbst oder Teile davon.
- DNA-Impfung: Der Bauplan des Eiweißes wird als Erbmaterial (DNA) geimpft. Die Zelle stellt dann das Eiweiß selbst her.
- mRNA-Impfung: Die Impfung enthält das Übersetzungs-Molekül (mRNA), das den Bauplan vom Zellkern in die Zelle bringt. Dieser Ansatz ist vor allem durch die Corona-Impfung bekannt geworden, wird aber auch in der Krebsmedizin intensiv erforscht. Die Zelle stellt das Eiweiß ebenfalls selbst her.
- Dendritische Zellen: Ein anderer Ansatz ist es, Immunzellen außerhalb des Körpers mit Tumorantigenen zu beladen. Dafür benutzt man Zellen, die weiteren Immunzellen solche Eiweiße zeigen und sie damit anregen, die Krebszellen zu bekämpfen. Sie heißen dendritische Zellen. Für die Behandlung werden sie der Patientin oder dem Patienten entnommen, vervielfältigt, beladen und wieder zurückgegeben.
Stellenwert: Diese Ansätze werden überwiegend noch erforscht, entweder in der Grundlagenforschung oder in vorklinischen oder klinischen Studien. In Deutschland gibt es derzeit keine zugelassenen Medikamente.
Teilweise sind erste Studien-Ergebnisse mit Impftherapien vielversprechend. Andere Ansätze haben sich als nicht wirksam genug erwiesen. Eine Schwierigkeit ist es, geeignete Tumorantigene zu finden. Außerdem muss die Impfantwort ausreichend verstärkt werden, um den Tumor effektiv zu bekämpfen. Geforscht wird deshalb auch an der Kombination von Tumorimpfungen mit anderen Therapien, zum Beispiel mit Checkpoint-Inhibitoren.
Unterschied: therapeutische oder vorbeugende Krebs-Impfung?
Therapeutische Impfung: Dabei werden Menschen geimpft, die bereits Krebs haben. Das Immunsystem soll auf die Krebszellen aufmerksam gemacht werden, um sie zu bekämpfen. Sie ist deshalb eine Form der Immuntherapie.
Vorbeugende Impfung: Es werden gesunde Menschen geimpft. Die Impfung soll eine Infektion mit dem jeweiligen Erreger verhindern, indem das Immunsystem auf diesen Erreger "trainiert" wird. Ein Beispiel ist die Impfung gegen Humane Papillomviren (HPV). Diese Viren können Krebs auslösen. Die Impfung schützt also vor der Infektion mit HPV und damit vor der Krebsentstehung. Mehr dazu unter HPV: Impfung gegen Humane Papillomviren.
Zytokine und weitere Immunmodulatoren
Als Immunmodulatoren bezeichnen Fachleute Stoffe, die das Immunsystem ungezielt beeinflussen können. Das können körpereigene oder künstlich hergestellte Stoffe sein. In der Krebsbehandlung spielen Immunmodulatoren inzwischen eine untergeordnete Rolle, werden aber bei manchen Krebsarten immer noch eingesetzt.
Zytokine
Zytokine sind Botenstoffe des Körpers, die häufig von Immunzellen ausgeschüttet werden. Sie tragen Namen wie Interferon oder Interleukin. Sie steuern zum Beispiel die Immunreaktion und können das Immunsystem anregen. Deshalb werden sie auch als Krebsmedikament verwendet. Allerdings ist ihre Wirkung gegen Krebs begrenzt und die Nebenwirkungen der Therapie können erheblich sein.
Stellenwert: Tumorarten, bei denen Zytokine infrage kommen, sind zum Beispiel Hautkrebs, Leukämien und Lymphome. Sie werden aber zunehmend von neueren Medikamenten abgelöst oder nur noch im Kombination mit anderen Behandlungsmethoden eingesetzt.
Ablauf der Therapie: Zytokine erhalten Betroffene als Infusion in eine Vene oder als Spritze unter die Haut. Wie häufig und wie lange die Behandlung stattfindet, hängt vom Wirkstoff ab.
Nebenwirkungen: Viele Betroffene haben während einer Therapie mit Zytokinen grippeähnliche Symptome, Durchfall oder Veränderungen der Haut oder des Blutbildes.
Thalidomid und ähnliche Medikamente
Thalidomid war in den 1960er Jahren unter dem Markennamen Contergan bekannt. Es wurde als Schlafmittel eingenommen und rief schwere Missbildungen bei Kindern hervor, deren Mütter es in der Schwangerschaft bekommen hatten.
Seit einigen Jahren wird Thalidomid in der Krebstherapie eingesetzt. Inzwischen gibt es verwandte Wirkstoffe wie Lenalidomid und Pomalidomid. Sie wirken unter anderem dadurch, dass sie die Ausschüttung von Zytokinen und die Aktivität verschiedener Immunzellen beeinflussen.
Stellenwert: Die Wirkstoffe sind zur Behandlung von Patientinnen und Patienten mit verschiedenen Tumorarten des blutbildenden und lymphatischen Systems zugelassen, zum Beispiel dem Multiplen Myelom.
Ablauf der Therapie: Die Medikamente werden einmal täglich als Kapseln geschluckt. Diese Therapie wird solange fortgesetzt, wie sie wirkt.
Nebenwirkungen sind beispielsweise Veränderungen des Blutbildes, Blutgerinnsel, Nervenschäden, Verdauungsstörungen und Wasseransammlungen im Gewebe. Außerdem wirken die Medikamente stark fruchtschädigend. Daher müssen Frauen im gebärfähigen Alter auf jeden Fall eine Schwangerschaft vermeiden und die Abgabe der Medikamente ist an strenge Auflagen gebunden.
Bacillus Calmette Guerin
Bacillus Calmette Guerin (BCG) ist ein abgeschwächter Stamm von Tuberkulose-Bakterien und wird auch als Tuberkulose-Impfstoff eingesetzt. BCG kann das körpereigene Immunsystem anregen und eine Immunreaktion gegen den Tumor auslösen. Daher wird es auch zur örtlichen Krebsbehandlung eingesetzt.
Stellenwert: Mit BCG werden Patientinnen und Patienten mit Harnblasenkrebs behandelt, bei denen nach einer Operation ein höheres Rückfallrisiko besteht. Die Behandlung soll verhindern, dass der Harnblasenkrebs zurückkehrt.
Ablauf der Therapie: Betroffenen wird über einen Katheter wiederholt mit dem Medikament die Harnblase gespült.
Nebenwirkungen: Nach der Behandlung können vorübergehend Beschwerden wie bei einer Blasenentzündung und grippeähnliche Symptome wie Fieber auftreten.
Sonderfall Virotherapie
Es gibt Viren, die natürlicherweise bevorzugt menschliche Krebszellen befallen. Andere können künstlich dazu gebracht werden. Zerstören sie die Tumorzellen nach der Infektion, dann sprechen Fachleute von onkolytischen Viren.
Zusätzlich aktivieren die Viren das Immunsystem, das daraufhin selbst virusinfizierte Tumorzellen zerstört. Einmal aktiviert, soll das Immunsystem auch nicht virusbefallene Krebszellen erkennen und vernichten.
Wichtig bei dieser Therapieform ist: Die benutzten Viren dürfen keine andere schwere Erkrankung (mehr) auslösen.
Erforscht werden zum Beispiel Parvoviren und Reoviren, die beim Menschen keine bekannten Erkrankungen hervorrufen. Adenoviren werden geprüft, weil viele von ihnen vergleichsweise harmlose Krankheiten auslösen. Weitere Beispiele sind gentechnisch veränderte und harmlos gemachte Masern- und Herpesviren.
Stellenwert: Die Virotherapie ist ein weitgehend experimenteller Ansatz. In Europa ist bisher nur ein Produkt zugelassen: Das Arzneimittel Imlygic® enthält ein gentechnisch verändertes Herpesvirus. Es ist für manche Patientinnen und Patienten mit fortgeschrittenem schwarzen Hautkrebs geeignet.
Für weitere Ansätze liegen vor allem Daten aus der Grundlagenforschung und aus frühen klinischen Studien vor. Teilweise gibt es ermutigende Ergebnisse. Viele Ansätze sind jedoch bisher nicht wirksam genug oder nicht dauerhaft wirksam. Deshalb versuchen Forschende mit verschiedenen Methoden, die Virotherapie wirksamer zu machen oder sie mit etablierten Therapien wie Chemo- oder Strahlentherapie zu kombinieren.
Ablauf der Therapie: Die Viren werden bei Imlygic® direkt in den Tumor gespritzt. Patientinnen und Patienten erhalten alle 2 bis 3 Wochen eine oder bei mehreren Tumoren/Metastasen auch mehrere Spritzen. Die Therapie wird solange fortgesetzt, wie sie wirkt und das Fortschreiten der Erkrankung aufhält.
Nebenwirkungen können vor allem grippale Symptome wie Fieber, Schüttelfrost, Übelkeit und Müdigkeit sein.
Quellen und Links für Interessierte und Fachkreise
Im Folgenden finden Sie eine Auswahl an hilfreichen Links zum Weiterlesen und Quellen, die für die Erstellung dieses Textes genutzt wurden.
Leitlinien
Leitlinien deutscher Fachgesellschaften zur Therapie verschiedener Krebsarten finden sich beim Leitlinienprogramm Onkologie und bei der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e.V. (AWMF). In den jeweils auf eine Tumorart bezogenen Leitlinien finden sich Informationen zum Stellenwert der Immuntherapie.
Rechtlicher Rahmen
In Deutschland unterliegen immuntherapeutische und gentherapeutische Ansätze der Aufsicht durch das Paul-Ehrlich-Institut (PEI), dem Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel. Insbesondere Virotherapien/Gentherapien dürfen nur unter besonderen Auflagen eingesetzt werden, auch nach der Zulassung.
Arzneimittel
Als Quelle für Aussagen zu Medikamenten hat der Krebsinformationsdienst aktuelle Fachinformationen der Hersteller herangezogen (über www.fachinfo.de; für Fachkreise zugänglich). Arzneimittelinformationen gibt es auch in weiteren deutschsprachigen Datenbanken (überwiegend kostenpflichtig, etwa www.pharmnet-bund.de/dynamic/de/arzneimittel-informationssystem/index.html). Auch das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) und die EU-Arzneimittelbehörde EMA bieten umfassende Arzneimittelinformationen an. Zum Stellenwert neuer Arzneimittel bietet das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen evidenzbasierte Berichte ("Frühe Nutzenbewertung nach AMNOG bzw. §35a, SGB V).
Fachartikel (Auswahl)
Akhatova A, Chan CK, Azizan A, Aimagambetova G. The Efficacy of Therapeutic DNA Vaccines Expressing the Human Papillomavirus E6 and E7 Oncoproteins for Treatment of Cervical Cancer: Systematic Review. Vaccines (Basel). 2021 Dec 31;10(1):53. doi: 10.3390/vaccines10010053.
Cook M, Chauhan A. Clinical Application of Oncolytic Viruses: A Systematic Review. Int J Mol Sci. 2020 Oct 12;21(20):7505. doi: 10.3390/ijms21207505.
Grigor EJM, Fergusson D, Kekre N, Montroy J, Atkins H, Seftel MD, Daugaard M, Presseau J, Thavorn K, Hutton B, Holt RA, Lalu MM. Risks and Benefits of Chimeric Antigen Receptor T-Cell (CAR-T) Therapy in Cancer: A Systematic Review and Meta-Analysis. Transfus Med Rev. 2019 Apr;33(2):98-110. doi: 10.1016/j.tmrv.2019.01.005.
Khoja L, Day D, Wei-Wu Chen T, Siu LL, Hansen AR. Tumour- and class-specific patterns of immune-related adverse events of immune checkpoint inhibitors: a systematic review. Ann Oncol. 2017 Oct 1;28(10):2377-2385. doi: 10.1093/annonc/mdx286.
Ma J, Mo Y, Tang M, Shen J, Qi Y, Zhao W, Huang Y, Xu Y, Qian C. Bispecific Antibodies: From Research to Clinical Application. Front Immunol. 2021 May 5;12:626616. doi: 10.3389/fimmu.2021.626616.
Marron TU, Ryan AE, Reddy SM, Kaczanowska S, Younis RH, Thakkar D, Zhang J, Bartkowiak T, Howard R, Anderson KG, Olson D, Naqash AR, Patel RB, Sachdev E, Rodriguez-Ruiz ME, Sheffer M, Church S, Fuhrman C, Overacre-Delgoffe A, Nguyen R, Florou V, Thaxton JE, Aggen DH, Guerriero JL. Considerations for treatment duration in responders to immune checkpoint inhibitors. J Immunother Cancer. 2021 Mar;9(3):e001901. doi: 10.1136/jitc-2020-001901.
Noori M, Yazdanpanah N, Rezaei N. Safety and efficacy of T-cell-redirecting bispecific antibodies for patients with multiple myeloma: a systematic review and meta-analysis. Cancer Cell Int. 2023 Sep 5;23(1):193. doi: 10.1186/s12935-023-03045-y.
Pasqui DM, Latorraca CDOC, Pacheco RL, Riera R. CAR-T cell therapy for patients with hematological malignancies. A systematic review. Eur J Haematol. 2022 Dec;109(6):601-618. doi: 10.1111/ejh.13851.
Perdyan A, Sobocki BK, Balihodzic A, Dąbrowska A, Kacperczyk J, Rutkowski J. The Effectiveness of Cancer Immune Checkpoint Inhibitor Retreatment and Rechallenge-A Systematic Review. Cancers (Basel). 2023 Jul 4;15(13):3490. doi: 10.3390/cancers15133490.
Zahedipour F, Hosseini SA, Astaneh M, Kesharwani P, Jaafari MR, Sahebkar A. Application of VEGF/VEGFR peptide vaccines in cancer: A systematic review of clinical trials. Crit Rev Oncol Hematol. 2023 Jul;187:104032. doi: 10.1016/j.critrevonc.2023.104032.