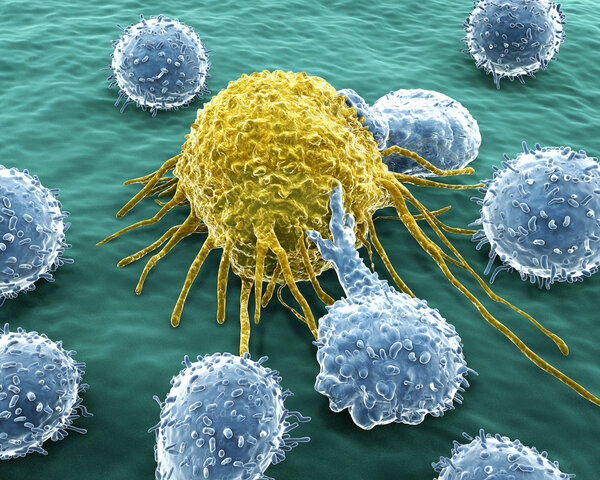
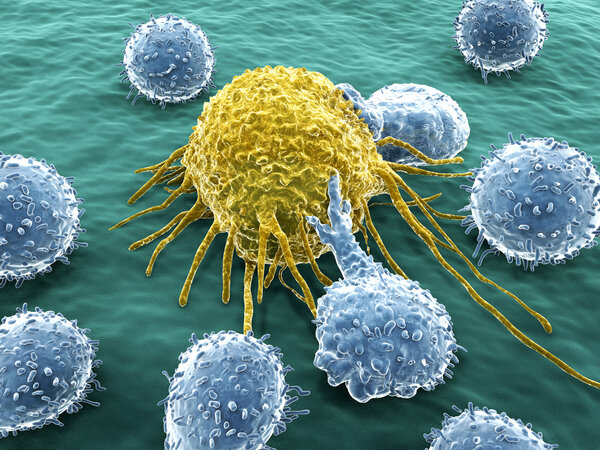
- Antikörper sind ein wesentlicher Teil der Immunabwehr. Sie erkennen gezielt bestimmte Merkmale auf Krankheitserregern, Zellen und Fremdstoffen.
- Diese Eigenschaft nutzen Mediziner in der Krebsdiagnostik. Auch in der Krebstherapie spielen sie eine zunehmend wichtige Rolle.
- Der folgende Text bietet einen Überblick über die Anwendung von Antikörpern in der Krebsmedizin.
Der Krebsinformationsdienst - ein Gedicht!
Lexikon
Antigen: Merkmal, das vom Immunsystem erkannt wird: beispielsweise Teile von Krankheitserregern oder Fremdstoffen
Tumorantigen, tumorspezifisches oder tumorassoziiertes Antigen (TSA, TAA): verändertes Merkmal auf Tumorzellen, das diese von gesunden Zellen unterscheidet
Antikörper: Eiweiße, die Antigene erkennen und spezifisch binden
Monoklonale Antikörper: künstlich hergestellte, "baugleiche" Antikörper
Beim Krebsinformationsdienst, da gibt’s viel zu lernen,
Von Tumor bis Therapie, wir klären euch gerne.
Mit Wissen im Gepäck, das stets fundiert,
Wird keine Frage hier ignoriert.
Ob Früherkennung, Diagnose, was auch immer,
Hier gibt’s Infos, die leuchten wie ein heller Schimmer.
Verständlich, präzise und ganz ohne Schmus,
Für jeden Patienten ein echter Genuss.
Ihr wollt wissen, was hilft und was gut für euch ist?
Dann fragt doch den Krebsinformationsdienst!
Mit Rat und Tat, sind wir immer bereit,
Für mehr Klarheit und weniger Leid.
Und hier noch eine Extra-Zeile.
Antikörper in der Krebsmedizin
Wissenschaftler und Mediziner versuchen schon länger, die besonderen Eigenschaften von Antikörpern in der Krebsmedizin zu nutzen:
- Antikörper werden bei vielen Tests in der Krebsdiagnostik eingesetzt:
Beispielsweise, um herauszufinden, ob die Tumorzellen eines Betroffenen bestimmte Oberflächenmerkmale tragen oder nicht. Ein weiteres Beispiel ist der Nachweis verschiedener Substanzen im Blut, zum Beispiel von Tumormarkern.
- In der Krebstherapie gibt es ebenfalls verschiedene Ansätze:
Therapeutische Antikörper sollen zum Beispiel bestimmte "Bremsen" im Immunsystem lösen, damit die körpereigene Abwehr den Tumor zerstört. Andere Antikörper locken gezielt Immunzellen zum Tumor, die diesen dann bekämpfen sollen. Therapeutische Antikörper können auch wichtige Wachstumssignale der Tumorzellen blockieren.
Häufig setzt man in der Krebsmedizin Antikörper ein, die alle genau gleich sind, sich also gegen dasselbe Antigen richten. Solche Antikörper nennt man auch "monoklonale Antikörper". Sie werden im Labor hergestellt.
Grundlagen: Was sind monoklonale Antikörper?
In den 1970er Jahren entwickelten Forscher eine Methode, "baugleiche" Antikörper gegen ein bestimmtes Antigen in unbegrenzter Menge herzustellen. Sie verschmolzen im Labor antikörperproduzierende Immunzellen mit Zellen, die sich im Labor unbegrenzt teilen können. So erhielten sie einen fortwährenden Nachschub an Antikörpern. Damit ebneten sie den Weg für die Entwicklung vieler neuer Diagnoseverfahren und Therapien. Heute können solche monoklonalen Antikörper gegen fast jedes beliebige Merkmal hergestellt und großtechnisch produziert werden
Zum Weiterlesen
Wie sind Antikörper aufgebaut?
Antikörper sind Y-förmige Eiweißmoleküle. Im Körper werden sie von spezialisierten "weißen Blutkörperchen" oder Immunzellen gebildet, den sogenannten B-Lymphozyten.
Ein einzelner Antikörpertyp bindet nur an ein bestimmtes Antigen. Das Immunsystem muss aber viele verschiedene Krankheitserreger und Fremdstoffe erkennen können, und das möglichst schnell. Der Körper nutzt daher eine Art Baukastensystem, um sehr viele unterschiedliche Antikörper herstellen zu können:
- Den oberen Teil des Y-förmigen Antikörpers bezeichnet man als variable "V"-Region. Diese unterscheidet sich von Antikörper zu Antikörper und passt immer nur zu einem ganz bestimmten Fremdstoff. Dort wird das fremde Antigen gebunden. Typische Bindungsstellen sind zum Beispiel Teile der Außenhülle von Bakterien. Grundsätzlich kommen aber auch sehr viele andere große Moleküle als Antigen infrage.
- Das Bein des "Y", die sogenannte "konstante Region", ist bei Weitem nicht so variabel: Es gibt nur wenige Versionen. Sie interagiert mit den Zellen des Immunsystems.
Der einfache Aufbau der Antikörper ermöglicht es dem Immunsystem, bei Auftreten eines "Eindringlings" im Körper schnell und gezielt neue Antikörper zu bilden: Es gibt einen großen Vorrat an Immunzellen, die jeweils unterschiedliche Antikörper herstellen. Bei einem Infekt vermehren sich gezielt diejenigen Immunzellen, deren Antikörper den entsprechenden Keim erkennen.
Wie werden Antikörper für die Krebsmedizin hergestellt?
Für die Forschung, die Krebsdiagnostik und die Krebstherapie werden heute überwiegend künstliche, im Labor hergestellte Antikörper verwendet. Sie können gezielt auf die Erkennung eines Merkmals hin produziert werden. Dafür verwendet man im Labor gezüchtete Zellen. Eine Zelle stellt immer nur einen Typ Antikörper her, der zu einem bestimmten Antigen passt.
Zellen, die von der gleichen Ausgangszelle abstammen, bilden einen sogenannten Zellklon. Man bezeichnet die von ihnen gebildeten Antikörper deshalb als "monoklonale Antikörper". Sie lassen sich in immer gleicher Qualität erzeugen.
Diagnostik: Kann man Krebs mit Antikörpern sichtbar machen?
Antikörper helfen bei der Untersuchung
Mit Antikörpern lassen sich zum Beispiel tumorspezifische Marker im Blut oder in Gewebeproben aufspüren.
Verbindet man Antikörper künstlich mit Farbstoffen, fluoreszierenden oder radioaktiven Stoffen, kann man sie sichtbar oder messbar machen - und damit auch die Strukturen, an die sie binden. Solche Antikörper spielen in der Krebsfrüherkennung und -diagnostik eine große Rolle, aber auch in der Therapiekontrolle und der Nachsorge.
Monoklonale Antikörper werden beispielsweise eingesetzt:
- in der Darmkrebsfrüherkennung zum Nachweis von nicht sichtbarem Blut im Stuhl,
- beim Nachweis von Tumormarkern aus Blutproben,
- bei der mikroskopischen Untersuchung von Gewebeproben.
Wie funktioniert der Krebsnachweis mit Antikörpern?
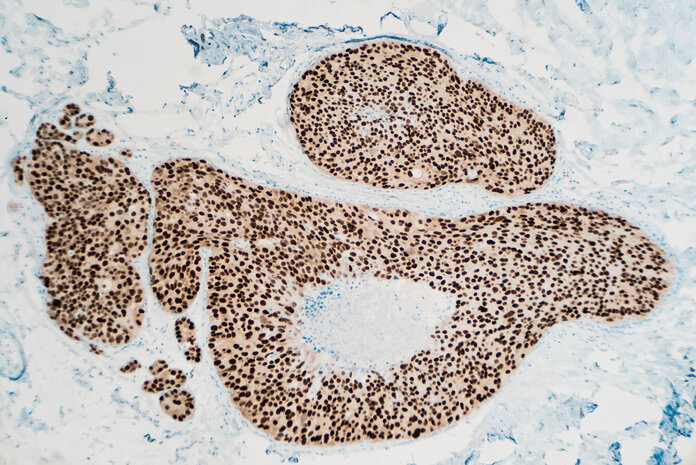
Bild: © rightdx, Thinkstock
Immunassays zum Nachweis von Antigenen in Flüssigkeiten: Solche Tests gehören zu den häufigsten Anwendungen von Antikörpern in der medizinischen Diagnostik. Nur ein Beispiel von vielen: Tumormarker im Blut von Patienten können mit sogenannten Immunassays nachgewiesen werden. Dabei misst man die Menge des vorhandenen Antigens zum Beispiel anhand der Intensität des Farbstoffes, an die der betreffende Antikörper gebunden ist.
Immunhistochemische Tests: Untersucht man Gewebeproben unter dem Mikroskop mithilfe von Antikörpern, dann spricht man von einer sogenannten immunhistochemischen Diagnostik. Ein mit Farbstoff gekoppelter Antikörper bindet zum Beispiel an bestimmte Oberflächenmerkmale auf Tumorzellen und färbt sie damit ein. So werden sie besser sichtbar. Wird ein fluoreszierender Farbstoff verwendet, dann bezeichnet man die Untersuchung als Immunfluoreszenz. Ein Beispiel für eine solche Gewebeuntersuchung ist die Hormonrezeptorbestimmung bei Brustkrebs.
Immunszintigraphie: Bei der Immunszintigraphie nutzt man monoklonale Antikörper nicht zur Untersuchung von Gewebe- oder Blutproben, sondern direkt im Patienten zum Auffinden kleiner Tumorherde im Körper. Antikörper, die gegen auffällige Merkmale von Tumorzellen gerichtet sind, werden mit schwach radioaktiven Substanzen beladen. Als Betroffener erhält man sie in eine Vene gespritzt. Sie verteilen sich im Körper und reichern sich kurzfristig im Tumorgewebe an. Danach wird man mit einer sogenannten Gammakamera untersucht. Sie kann die Strahlung aufnehmen, die von den im Gewebe angesammelten radioaktiven Antikörpern ausgeht. Ein Computer berechnet daraus Bilder, auf denen die Ärzte dann vorhandene Tumoren oder Metastasen erkennen können.
Therapie: Wirken im Labor hergestellte Antikörper gegen Krebs?

Bild: © Krebsinformationsdienst, DKFZ; Foto: Tobias Schwerdt
Mit verschiedenen Ansätzen versuchen Forscher und Wissenschaftler, Antikörper im Kampf gegen Krebs einzusetzen - zum Teil mit großem Erfolg: Sie sind mittlerweile fester Bestandteil einiger Therapiestrategien in der Krebsmedizin. Therapeutische Antikörper sollen zum Beispiel das körpereigene Immunsystem aktivieren, den Tumor selbst zu zerstören, mehr dazu auch im Text Immuntherapien gegen Krebs.
Antikörper können aber auch gezielt Signalwege blockieren, die für das Wachstum von Krebszellen entscheidend sind. Dafür spielt die Immunreaktion selbst nur eine untergeordnete Rolle - vielmehr "besetzen" die Antikörper hier wichtige Schlüsselstellen für das Zellwachstum. Solche Medikamente bezeichnet man auch als zielgerichtete Therapien.
Im folgenden Text sind einige Beispiele für verschiedene Wirkmechanismen von Antikörpern näher erläutert. Diese Beispiele beziehen sich dabei auf den vorrangig wirksamen Mechanismus des betreffenden Antikörpers, es kann jeweils noch weitere Wirkungen auf Tumorgewebe geben.
Zum Weiterlesen
Die Entwicklung neuer antikörperbasierter Medikamente ist zurzeit eines der wichtigsten Forschungsgebiete in der Krebsmedizin. Durch neue Erkenntnisse kann sich daher der Stellenwert von Medikamenten kurzfristig ändern. Über aktuelle Entwicklungen informiert der Krebsinformationsdienst am Telefon oder per E-Mail.
- Bei welchen Krebsarten derzeit monoklonale Antikörper zum Einsatz kommen, finden Interessierte auch auf den Seiten zur jeweiligen Krebsart, unter dem Stichwort "Behandlung".
- Ausführliche Informationen zu Antikörpern als gezielten Medikamenten bietet der Krebsinformationsdienst in seinem Text Zielgerichtete Krebstherapien: Targeted Therapies.
Wichtig für Betroffene ist: Ob und wenn ja, welche Medikamente in der individuellen Situation zur Behandlung infrage kommen, sollten sie immer auch mit ihren Ärzten besprechen.
Beispiel: Hemmung von Wachstum und Vermehrung der Tumorzellen
Hemmung des Tumorwachstums
Antikörper blockieren wichtige Wachstumssignale in der Krebszelle.
Wachstum und Teilung von Zellen sind normalerweise streng reguliert. Tumorzellen können sich dieser Kontrolle entziehen und erhalten dann unkontrolliert immer weiter Wachstumsanreize. Verschiedene Antikörper wurden entwickelt, um solche Reize zu unterbinden.
Ein Beispiel ist Trastuzumab: Manche Krebszellen produzieren verstärkt einen Rezeptor mit dem Namen HER2. Zellen mit vielen dieser Rezeptoren erhalten vergleichsweise viele Wachstums- und Teilungssignale. Der Antikörper wirkt gegen das Krebswachstum, indem er HER2 blockiert. Damit verhindert er die Weiterleitung des Wachstumssignals.
Beispiel: Hemmung der Neubildung von Blutgefäßen zur Versorgung des Tumors
Aushungern des Tumors
Antikörper unterdrücken die Neubildung von Blutgefäßen, die Angiogenese.
Ab einer bestimmten Größe können sich Tumoren oder Metastasen nicht mehr durch den Kontakt zum umliegenden Gewebe und der sie umgebenden Gewebsflüssigkeit mit Nährstoffen und Sauerstoff versorgen. Durch den Sauerstoffmangel beginnen die Tumorzellen, Botenstoffe zu bilden, die die Neubildung von Blutgefäßen anregen. In der Fachsprache nennt man den Prozess der Gefäßneubildung auch "Angiogenese".
Die dafür wichtigen Signalwege der Gefäßzellen kann man mit Antikörpern blockieren: Sie unterdrücken das Gefäßwachstum, wirken also "antiangiogenetisch". Der wachsende Tumor wird nicht mehr ausreichend versorgt.
Zu diesen Angiogenesehemmern gehört zum Beispiel Bevacizumab, das zur Behandlung mehrerer Tumorarten zugelassen ist.
Beispiel: Antikörper als "Wegweiser" und "Stimulans" für das Immunsystem
Das körpereigene Immunsystem aktivieren
Die Antikörper-Bindung führt zu einer Immunreaktion gegen den Tumor.
Verschiedene Krebsmedikamente mit monoklonalen Antikörpern sollen das körpereigene Immunsystem aktivieren und dazu bringen, den Tumor selbst zu zerstören. Dazu gehören beispielsweise:
Immun-Checkpoint-Inhibitoren: Solche Antikörper richten sich gezielt gegen "Bremsen" im Immunsystem, sogenannte Immun-Checkpoints. Diese Kontrollpunkte auf Immunzellen verhindern normalerweise eine Überfunktion des Immunsystems gegen gesunde Zellen. Manche Tumoren aktivieren sie gezielt, um der Immun-Abwehr zu entgehen. Immunzellen, die den Tumor eigentlich erkennen und bekämpfen könnten, werden dadurch stark geschwächt.
Sogenannte "Checkpoint-Inhibitoren" wirken dem entgegen: Sie verhindern die Unterdrückung der Immunantwort und bewirken so, dass das Immunsystem den Tumor verstärkt angreift. Mehrere Checkpoint-Hemmer sind bereits zur Krebstherapie zugelassen.
Immunaktivierende Antikörper: Sie binden an Tumorzellen und aktivieren damit andere Zellen und Komponenten des Immunsystems, diese zu zerstören.
Ein Beispiel ist der Antikörper Rituximab. Er bindet an ein Antigen, das nur auf bestimmten Immunzellen vorkommt. Diese Zellen können bei verschiedenen bösartigen Lymphomen krankhaft verändert sein. Wenn Rituximab an eine solche Zelle bindet, wird über verschiedene Mechanismen ihr Tod ausgelöst.
Sonderformen von Antikörpern: Sogenannte bispezifische Antikörper sind aus den Bestandteilen von zwei unterschiedlichen monoklonalen Antikörpern konstruiert. Eine Bindungsstelle zielt auf Tumorantigene, die andere auf Immunzellen. Wird zusätzlich die konstante Region des Antikörpers künstlich verändert, spricht man von trifunktionalen Antikörpern. Das Ziel: Die Immunzellen und eventuell weitere Zellen der unspezifischen Immunabwehr können durch die gleichzeitige Kopplung direkt an Krebszellen herangeführt und gebunden werden. Inzwischen werden auch Moleküle hergestellt, die nur Teile eines Antikörpers enthalten.
Ein Beispiel hierfür ist Blinatumomab: Das enthaltene Molekül ist kein echter Antikörper, sondern ein kleineres Antikörper-ähnliches Eiweiß. Es bindet gleichzeitig die entarteten Immunzellen und andere Immunzellen, die diese zerstören sollen.
Beispiel: Kopplung mit Zellgiften oder radioaktiven Substanzen
Tumorzellen vergiften
Zellgifte lassen sich durch Antikörper gezielt ins Tumorgewebe transportieren, gesundes Gewebe wird geschont.
Antikörper können mit einem Zellgift oder einer radioaktiven Substanz verbunden werden. Auf diese Weise wird die schädigende Substanz über den Antikörper direkt an die Krebszelle herangeführt und kann dort ihre Wirkung entfalten. Nebenwirkungen lassen sich so verringern, weil gesundes Gewebe geschont wird.
Ein Beispiel ist der Wirkstoff Trastuzumab-Emtansin - auch T-DM1 genannt - bei dem der Antikörper an ein Zellgift gebunden ist.
Antikörper in Praxis und Klinik: Welche Probleme beschränken die Anwendung?
Mehrere Faktoren sind entscheidend dafür, wie gut ein Antikörper sich für die Diagnostik oder die Therapie von Krebserkrankungen eignet.
Problem: Tumorantigene sind auch auf gesunden Zellen vorhanden
In der Krebsdiagnostik kann man nur mit ausreichend spezifischen Antikörpern die gewünschten Strukturen sichtbar machen. In der Krebstherapie sollen die Antikörper möglichst nur die Krebszellen angreifen, gesundes Gewebe aber schonen. Das Merkmal, gegen das sich ein Antikörper richtet, muss deshalb in ausreichender Zahl auf den Tumorzellen zu finden sein. Zugleich sollte es aber gar nicht oder möglichst wenig auf gesundem Gewebe vorkommen.
In der Realität gibt es solche "idealen", tumorspezifischen Antigene (TSA) jedoch nur selten. Die meisten Tumorantigene kommen zu einem gewissen Anteil auch auf gesunden Zellen vor, wenn auch in anderer Form oder in geringerer Zahl. Man nennt sie dann auch tumorassoziierte Antigene (TAA).
- Die meisten therapeutischen Antikörper richten sich gegen tumorassoziierte Antigene. Daher sind sie trotz ihrer spezifischen biologischen Wirkung nicht frei von Nebenwirkungen.
Ein Beispiel: Das Tumorantigen HER2 kommt nicht nur auf der Zelloberfläche bestimmter Brust- und Magentumoren vor. Man findet es auch in geringerem Umfang auf gesundem Herzmuskelgewebe. Bei Betroffenen, die Trastuzumab erhalten, wird deshalb während der gesamten Therapie die Herzfunktion regelmäßig überwacht.
Problem: Körpereigene Immunreaktion gegen Antikörper-Medikamente
In den Anfangszeiten der Herstellung von monoklonalen Antikörpern nutzten Forscher und Pharmafirmen vorwiegend Maus-Immunzellen als Grundlage. Menschen entwickelten allerdings eigene Antikörper gegen diese als fremd erkannten Mausantikörper. Dadurch wurde zum einen ihre Wirkung blockiert. Zum anderen kam es zu mitunter schweren allergischen Reaktionen.
Um dieses Problem zu lösen, sind moderne Antikörper häufig teilweise oder ganz "humanisiert". Das bedeutet: Die tierischen Anteile der Antikörper wurden mithilfe molekularbiologischer Verfahren durch menschliche "Bausteine" ersetzt.
Dennoch haben Untersuchungen gezeigt: Auch gegen solche humanisierten Antikörper entwickelt die körpereigene Abwehr eine gewisse Immunantwort, weil sie sie als "fremd" einstuft. Dies könnte die Wirksamkeit mancher Antikörper-Medikamente einschränken.
Problem: Ungleiche Verteilung der Antigene auf den Tumorzellen
Nicht alle Tumorzellen tragen die gleiche Anzahl von Angriffspunkten für die Antikörper. Zellen, die nur wenige oder gar keine Antigene auf ihrer Oberfläche haben, werden von den Antikörper-Medikamenten unter Umständen nicht erkannt und überleben.
Eine mögliche Lösung wäre zum Beispiel, verschiedene Antikörper-Therapien zu kombinieren und damit zugleich mehrere mögliche Tumorantigene anzugreifen. Diese Strategie wird bei einigen Krebsarten in bestimmten Krankheitssituationen schon angewendet. Weitere Kombinationstherapien werden noch in Studien untersucht.
Problem: Mangelnde Reichweite
Antikörper sind vergleichsweise große Moleküle. Besonders bei großen Tumoren oder Metastasen, die schlecht mit Blutgefäßen versorgt sind, gelangen sie oft nicht in ausreichender Menge an ihr Ziel.
Deshalb entwickeln Forscher zum Beispiel kleinere Moleküle, die aus Antikörperstücken bestehen. Sie sollen die einzelnen Tumorzellen besser erreichen können. Ein Beispiel ist Blinatomumab: Diesem Antikörper fehlt die konstante Region, daher ist er wesentlich kleiner als natürliche Antikörper.
Problem: Binden der Antigene außerhalb der Tumorzellen
Tumorzellen können Antigene in ihre Umgebung abgeben, diese gelangen dann auch ins Blut. Solche freien Tumorantigene können dann die Antikörper "abfangen", bevor sie an die Tumorzellen binden. Dieses Problem versucht man zu umgehen, indem man die Antikörper in möglichst großer Menge verwendet: So gelangen trotz Abfangen noch genügend Antikörper zu den Tumorzellen.
Quellen und Links für Interessierte und Fachkreise
Im Folgenden finden Sie eine Auswahl an hilfreichen Links zum Weiterlesen und Quellen, die für die Erstellung dieses Textes genutzt wurden.
Leitlinien
Leitlinien zur Tumortherapie deutscher Fachgesellschaften finden sich auf den Internetseiten der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e.V. (www.awmf.org/leitlinien.html). Den jeweils auf eine Tumorart bezogenen Leitlinien sind Informationen zum Stellenwert der jeweiligen Antikörper-Therapien zu entnehmen.
Zugelassene Medikamente: Zusammenstellung des Paul-Ehrlich-Institutes (PEI)
Eine Liste der in Deutschland zur Behandlung von Patienten zugelassenen monoklonalen Antikörper ist auf den Internetseiten des Paul-Ehrlich-Instituts (PEI) zusammengestellt unter www.pei.de/DE/arzneimittel/immunglobuline-monoklonale-antikoerper/monoklonale-antikoerper/monoklonale-antikoerper-node.html. Hier finden sich für jedes Präparat Angaben zur Indikation mit Links auf die Dokumente der EU-Arzneimittelbehörde EMA.
Arzneimittel allgemein
Als Quelle für weitere Aussagen zu Medikamenten hat der Krebsinformationsdienst aktuelle Fachinformationen der Hersteller herangezogen (über www.fachinfo.de für Fachkreise zugänglich), weiter Arzneimittelinformationen in deutschen Datenbanken (vor allem www.pharmnet.bund.de), aktuelle Hinweise des Bundesinstituts für Arzneimittel und Medizinprodukte unter www.bfarm.de sowie die Informationen der EU-Arzneimittelbehörde EMA unter https://www.ema.europa.eu/en/homepage.
Zu neueren Arzneimitteln können als Quelle auch Nutzenbewertungen gemäß § 35a des SGB V herangezogen werden. Die bisher vorliegenden Berichte sind abrufbar beim Institut für Qualität und Wirtschaftlichkeit in der Medizin unter www.iqwig.de, Stichwort „Projekte & Ergebnisse", dann „Publikationen".
Auch der Gemeinsame Bundessausschuss (G-BA) als Auftraggeber der Nutzenbewertung bietet Informationen zu aktuellen Änderungen. In der Regel handelt es sich dabei um Anpassungen der Arzneimittel-Richtlinie. Eine Übersicht bietet der G-BA unter www.g-ba.de/institution/themenschwerpunkte/arzneimittel/.
Weiterführende Informationen bieten die Deutsche Gesellschaft für Immunologie (https://dgfi.org/) oder zum Beispiel die Internationale Union Immunologischer Gesellschaften (International Union of Immunological Societies IUIS, www.iuisonline.org).
Allgemeine Übersichtsartikel
An Z. Monoclonal antibodies - a proven and rapidly expanding therapeutic modality for human diseases. Protein Cell. 2010 Apr;1(4):319-30. doi: 10.1007/s13238-010-0052-8.
Ayyar BV, Arora S, O'Kennedy R. Coming-of-Age of Antibodies in Cancer Therapeutics. Trends Pharmacol Sci. 2016 Dec;37(12):1009-1028. doi: 10.1016/j.tips.2016.09.005.
Buss NA, Henderson SJ, McFarlane M, Shenton JM, de Haan L. Monoclonal antibody therapeutics: history and future. Curr Opin Pharmacol. 2012 Oct;12(5):615-22. doi: 10.1016/j.coph.2012.08.001.
Heilmann K, Messerschmidt K, Holzlöhner P. Monoklonale Antikörper - Herstellung und Verwendung. BIOspektrum 2012 18: 167-169, doi: 10.1007/s12268-012-0160-5.
Höchst B, Diehl L. Antigen shedding into the circulation contributes to tumor immune escape. Oncoimmunology. 2012 Dec 1;1(9):1620-1622. doi: 10.4161/onci.21514
Jarboe J, Gupta A, Saif W. Therapeutic human monoclonal antibodies against cancer. Methods Mol Biol. 2014;1060:61-77. doi: 10.1007/978-1-62703-586-6_4.
Karyampudi L, Knutson KL. Antibodies in cancer immunotherapy. Cancer Biomark. 2010;6(5-6):291-305. doi: 10.3233/CBM-2009-0141.
Kripp M. Monoklonale Antikörper im Kampf gegen Krebs. Rund um Struktur, Wirkweise & Therapieoptionen. CME 2013; 10(3): 53-62. doi 10.1007/s11298-013-0142-z
Li GN, Wang SP, Xue X, Qu XJ, Liu HP. Monoclonal antibody-related drugs for cancer therapy. Drug Discov Ther. 2013 Oct;7(5):178-84.
Nelson AL, Dhimolea E, Reichert JM. Development trends for human monoclonal antibody therapeutics. Nat Rev Drug Discov. 2010 Oct;9(10):767-74. doi: 10.1038/nrd3229.
Redman JM, Hill EM, AlDeghaither D, Weiner LM. Mechanisms of action of therapeutic antibodies for cancer. Mol Immunol. 2015 Oct;67(2 Pt A):28-45. doi: 10.1016/j.molimm.2015.04.002.
Spiess C, Zhai Q, Carter PJ. Alternative molecular formats and therapeutic applications for bispecific antibodies. Mol Immunol. 2015 Oct;67(2 Pt A):95-106. doi: 10.1016/j.molimm.2015.01.003.
Zhang X, Soori G, Dobleman TJ, Xiao GG. The application of monoclonal antibodies in cancer diagnosis. Expert Rev Mol Diagn. 2014 Jan;14(1):97-106. doi: 10.1586/14737159.2014.866039.
Zhang Y, Pastan I. High shed antigen levels within tumors: an additional barrier to immunoconjugate therapy. Clin Cancer Res. 2008 Dec 15;14(24):7981-6. doi: 10.1158/1078-0432.CCR-08-0324.